Khi tìm hiểu tính chất vật lý của các chất hay hợp chất chắc rằng chúng ta đều thấy xuất hiện yếu tố độ tan. Vậy độ tan là gì? Ngay sau đây mayruaxegiadinh.com.vn sẽ giúp bạn hiểu được khái niệm về yếu tố này cũng như công thức tính độ tan, đặc điểm độ tan trong nước của một số chất hay các muối tan và không tan,…. Cùng theo dõi nhé!
Contents
Độ tan là gì?
Khái niệm
Độ tan được hiểu đơn giản là một đại lượng đặc trưng cho khả năng hòa tan của một chất (rắn, lỏng hoặc khí) vào dung môi để có thể tạo thành một dung dịch đồng nhất. Độ tan còn được hiểu theo cách khác chính là số gam của chất đó có khả năng hòa tan vào trong 100g dung môi (thường là nước) để tạo ra dung dịch bão hòa tại một điều kiện nhiệt độ bất kỳ cho trước.

Để xác định một chất tan hay không tan người ta thường dựa vào một số đặc trưng cụ thể như sau:
- Nếu chất đó hòa tan được vào trong 100g nước từ 10g trở lên thì được gọi là chất tan hay chất dễ tan.
- Nếu chất đó hòa tan được vào trong 100g nước dưới 1g thì được gọi là chất ít tan.
- Nếu chất đó hòa tan được vào trong 100g nước dưới 0,01g thì được gọi là chất không tan.
Độ tan của muối, axit và bazơ trong nước
– Hầu hết các axit ngoại từ axit silixic (H2SiO3) đều tan được trong nước.
– Các bazơ phần lớn đều không tan trong nước, ngoại từ các bazơ như: NaOH, Ba(OH)2, KOH,… và Ca(OH)2 là ít tan.
– Muối:
- Tất cả các muối K, Na và muối nitrat (_NO3) đều tan.
- Các muối clorua và sunfat đa số đều tan được và các muối cacbonat phần lớn là không tan.
Công thức tính độ tan
Công thức tính độ tan của các chất cụ thể là:
S = (mct/mdm) . 100
Trong đó:
– Ký hiệu của độ tan là S
– Khối lượng của chất rắn cần tính độ tan là mct
– Khối lượng của dung môi là mdm.
Ví dụ: Cho muối Na2CO3 hãy xác định độ tan của muối này khi ở nhiệt độ 18℃. Biết rằng, ở nhiệt độ này thì với 250g nước sẽ hòa tan được hết 53g muối Na2CO3 và thu được dung dịch bão hòa.
Giải: Ta có: SNa2CO3 = 53. 100/250 = 21,2

Chúng ta có thể đưa ra kết luận về mối quan hệ giữa độ tan của một chất với nồng độ phần trăm dung dịch bão hòa của chúng từ công thức trên ở một nhiệt độ xác định như sau:
C = 100 . S/(100+S)
Độ tan càng lớn tương ứng với chất tan càng mạnh và ngược lại độ tan càng nhỏ thì chất đó càng tan kém.
Độ tan phụ thuộc vào yếu tố nào?
Ngoài 2 yếu tố chính goomg nhiệt độ và áp suất như đã nói ở phần khái niệm thì độ tan của một chất còn phụ thuộc vào các yếu tố khác như: độ phân cực của chất tan và dung môi, dạng thù hình, hiện tượng hydrat hóa hiện tượng đa hình, độ pH của dung dịch, chất điện li, các ion cùng tên và hỗn hợp dung môi.
Nhiệt độ
Đối với chất khí, nhiệt độ tỷ lệ nghịch với độ tan của nó trong dung môi, độ tan của chất khí tăng nếu nhiệt độ giảm. Vì thế chúng ta có thể tiến hành đun nóng chúng để có thể loại bỏ được các chất khí như O2 hay khí CO2 ra khỏi dung môi. Và trong cách làm này thì không làm biến đổi hay phân hủy chất, đặc biệt còn giữ được độ ổn định cho dược chất.
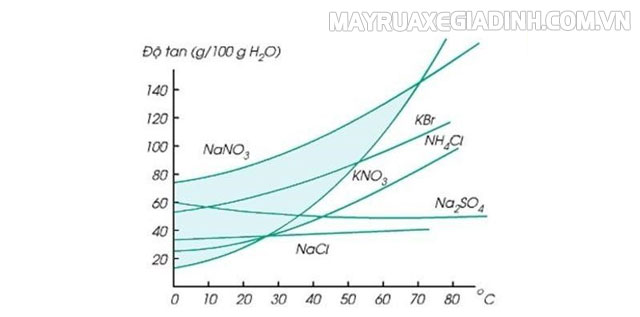
Đối với chất rắn thì ngược lại, nhiệt độ tỷ lệ thuận với độ tan. Do đó, các chất rắn thu nhiệt khi hòa tan thì nhiệt độ càng cao kéo theo độ tan sẽ càng lớn còn đối với chất rắn tỏa nhiệt thì ngược lại, nhiệt độ càng cao đồng nghĩa với độ tan của chúng sẽ càng giảm.
Áp suất (xác định với chất khí)
Theo định luật Henry thì các chất khí có độ tan nhỏ đồng thời có áp suất không quá cao thì lượng chất khí hòa tan trong một thể tích chất lỏng xác định thường có tỷ lệ thuận với áp suất của nó trên một bề mặt chất lỏng ở một nhiệt độ xác định không đổi.
Do đó, độ tan của chất khí sẽ tăng nếu tăng áp suất và ngược lại, nếu giảm áp suất thì độ tan của chất khí đó sẽ giảm đi.
Độ phân cực của chất tan và dung môi
Các chất phân cực có độ tan lớn hay tan dễ trong các dung môi phân cực điển hình như: nước, dung dịch muối, axit vô cơ, kiềm,….
Các chất ít phân cực thì lại dễ tan hơn trong những dung môi hữu cơ kém phân cực điển hình như: chloroform, toluene, benzene, dicloromethan,….
Dạng thù hình
So với các chất rắn tinh thể thì các chất rắn dạng vô định hình sẽ có độ tan lớn hơn. Lý do là vì ở dạng kết tinh thì có cấu trúc mạng lưới tinh thể tương đối bền vững vì thế mà nó cần có nhiều năng lượng hơn để có thể phá vỡ cấu trúc hơn.
Tuy nhiên, các chất rắn ở dạng vô định hình thường không ổn định như dạng tinh thể nên có xu hướng chuyển sang dạng tinh thể.

Hiện tượng hydrat hóa
Chất rắn trong quá trình kết tinh có thể tồn tại dưới dạng khan hoặc ngậm nước. Chất rắn ở dạng khan so với dạng ngậm nước có độ tan thấp hơn.
Hiện tượng đa hình
Một số chất rắn tùy vào điều kiện xảy ra kết tinh mà có các dạng tinh thể khác nhau như: đồng kết tinh hay hydrat,… có các tính chất vật lý cũng như độ tan trong dung môi là khác nhau. Đối với những tinh thể kém bền thường dễ tan hơn bởi chúng sẽ cần ít năng lượng trong phá vỡ cấu trúc.
Độ pH của dung dịch
- Độ tan của axit yếu sẽ tăng lên khi kiềm hóa dung môi.
- Các chất kiềm yếu sẽ có độ tan tăng lên khi axit hóa dung môi.
- Độ pH của các chất lưỡng tính càng gần điểm đẳng điện thì độ tan sẽ càng giảm và ngược lại độ tan sẽ tăng lên khi độ pH càng xa điểm đẳng điện đó.
Chất điện ly
Độ tan của các chất tan có thể bị giảm đi bởi chất điện ly trong dung dịch bởi thế trước khi hòa vào dung dịch cần lưu ý để pha loãng chất điện ly trước.
Các ion cùng tên
Cân bằng điện ly của chất tan sẽ dần chuyển dịch về hường phân tử ít tan khi nồng độ của các ion cùng tên tăng nên, đồng thời làm giảm đi độ tan của chất. Do đó, cần tiến hành với các chất ít tan trước rồi mới đến các chất dễ tan khi thực hiện việc hòa tan.
Hỗn hợp dung môi
Độ tan của các chất khó tan sẽ tăng lên nếu kết hợp những hỗn hợp dung môi đồng tan cùng với nước điển hình như glycerin-ethanol-nước.
Bảng độ tan của một số chất
Bảng độ tan của muối, axit, bazơ
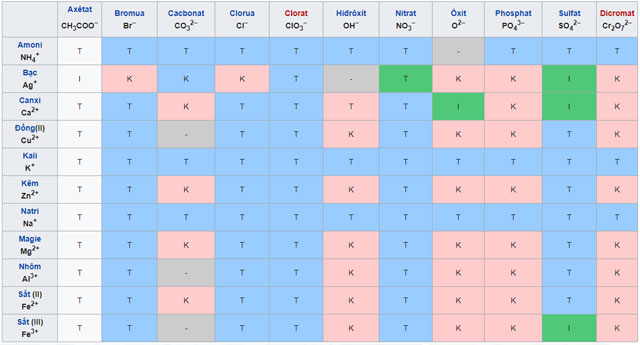
Bảng độ tan của Hiđro và các kim loại.
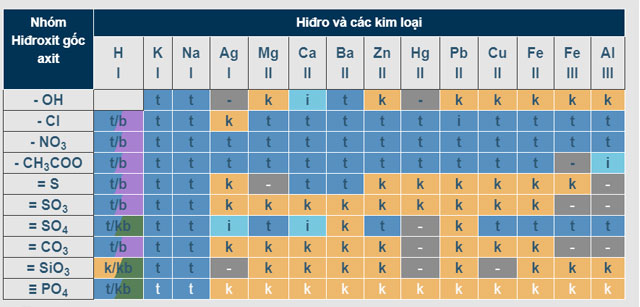
Trong đó:
- T: chất dễ tan
- I: chất ít tan
- K: chất không tan
- B: chất bay hơi
- (-): chất sẽ bị nước phân hủy hoặc không tồn tại.
Một số dạng bài tập về độ tan
Cùng tìm hiểu hiểu một số dạng bài tập liên quan để hiểu hơn về độ tan là gì và áp dụng công thức tính độ tan trong phần dưới đây nhé!
Dạng 1: Tính lượng tinh thể ngậm nước cần để cho thêm vào dung dịch
Cách giải:
Đầu tiên ta cần áp dụng định luật bảo toàn khối lượng để tính: mddtt = mtt + mddbd
Trong đó:
- mddtt là khối lượng của dung dịch tạo thành.
- mtt là khối lượng tinh thể.
- mddbd là khối lượng ban đầu của dung dịch.
Sau đó, áp dụng công thức tính khối lượng của chất tan trong dung dịch tạo thành: m = mcttt + mctbd
Trong đó:
- mcttt là khối lượng chất tan có trong tinh thể.
- mctbd là khối lượng chất tan ban đầu có trong dung dịch.
Thông thường đề bài sẽ cho sẵn loại tinh thể cần lấy cũng như dung dịch cho sẵn có chứa cùng loại chất tan đối với các dạng tính lượng tinh thể ngậm nước này.
Dạng 2: Tính lượng chất tan cần thêm vào hoặc tách ra khi thay đổi nhiệt độ.
Cách giải:
- Tính khối lượng của chất tan và dung môi có trong dung dịch bão hòa ở nhiệt độ (t1).
- Đặt ẩn số: khối lượng chất tan A được tìm sau khi thay đổi nhiệt độ là a(g).
- Tính lượng chất tan và dung môi có trong dung dịch bão hòa khi ở nhiệt độ t2.
- Áp dụng công thức C% hay công thức tính độ tan trong dung dịch bão hòa để tìm ra ẩn a.
Tuy nhiên, với dạng bài toán này thì khi được yêu cầu tính lượng tinh thể ngậm nước phải thêm vào hay được tách ra bởi yếu tố nhiệt độ thay đổi, ta cần phải đặt ẩn số là số mol (n) thay vì đặt số gam.
Kết Luận
Như vậy chúng ta đã vừa tìm hiểu độ tan là gì cũng như công thức tính độ tan, đặc điểm độ tan của một số chất trong nước. Hy vọng rằng những thông tin trên đây sẽ giúp bạn củng cố thêm phần kiến thức này một cách chi tiết.
Cảm ơn bạn đã dành thời gian cho bài viết, theo dõi mayruaxegiadinh.com.vn để cập nhật nhanh nhiều hơn các kiến thức thú vị bạn nhé!



